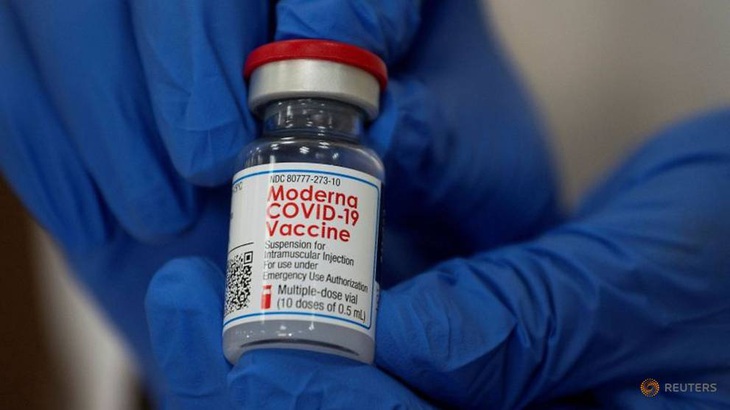
Một lọ vắc xin COVID-19 của Hãng Moderna tại một bệnh viện ở bang New York, Mỹ ngày 21-12-2020 - Ảnh: REUTERS
Vắc xin Moderna, còn có tên là Skipevax, mỗi liều 0,5ml chứa 100mcg mRNA, được nhúng trong các lipid nanoparticle SM-102, dạng bào chế là hỗn dịch tiêm bắp, hộp chứa 10 lọ đa liều, mỗi lọ đa liều chứa 10 liều 0,5mcg, cơ sở sản xuất là Rovi Pharma (Tây Ban Nha) và Recipharm (Monts, Pháp) vừa được Bộ Y tế ký quyết định phê duyệt có điều kiện tại Việt Nam.
Quyết định phê duyệt này kèm theo 9 điều kiện: đơn vị nhập khẩu phối hợp với Cục Khoa học, công nghệ và đào tạo tổ chức đánh giá an toàn và hiệu quả của vắc xin; phối hợp đơn vị phân phối và sử dụng triển khai theo dõi cảnh giác dược.
Đồng thời phối hợp với Bộ Y tế triển khai kiểm định vắc xin trước khi ra thị trường và quản trị rủi ro trong suốt quá trình vắc xin lưu hành tại Việt Nam.
Moderna là vắc xin ngừa COVID-19 thứ 5 được phê duyệt có điều kiện để sử dụng tại Việt Nam tính từ tháng 2 đến nay. Theo thông tin từ Bộ Y tế, đã có một đơn vị ký hợp đồng nhập khẩu 5 triệu liều Moderna về Việt Nam.
Dịp này, Bộ Y tế cũng cho biết nhóm nghiên cứu thử nghiệm lâm sàng vắc xin Covivax đã gửi mẫu đánh giá hiệu quả sinh kháng thể sau giai đoạn 1 thử nghiệm lâm sàng tại Canada.
Kết quả thử nghiệm giai đoạn 1 bước đầu cho thấy vắc xin an toàn và có hiệu quả đáng kể, chuẩn bị báo cáo Hội đồng đạo đức trong nghiên cứu y sinh để chuyển sang giai đoạn 2 thử nghiệm lâm sàng tại Thái Bình. Đây là ứng viên vắc xin có tiến độ nhanh thứ 2 trong số các vắc xin ngừa COVID-19 đang phát triển tại Việt Nam.











Tối đa: 1500 ký tự
Hiện chưa có bình luận nào, hãy là người đầu tiên bình luận