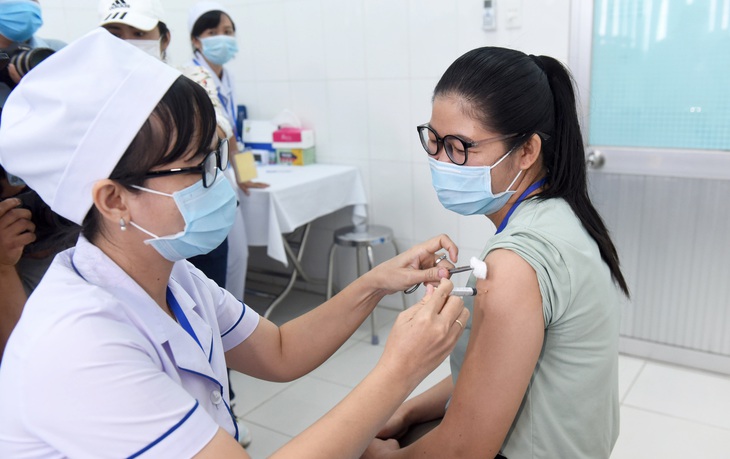
Tiêm thử nghiệm vắc xin Nano Covax ngừa COVID-19 cho tình nguyện viên tại tỉnh Long An - Ảnh: DUYÊN PHAN
Dự kiến hoạt động lấy mẫu sẽ kéo dài đến đầu tuần tới, nhưng các mẫu đã lấy từ giữa tháng 7 đến nay đã được chuyển đến đơn vị phụ trách đánh giá kết quả (Viện Vệ sinh dịch tễ trung ương).
Nhóm nghiên cứu cũng cho biết đang gấp rút hoàn thiện các biểu mẫu để gửi báo cáo dữ liệu thử nghiệm lâm sàng giai đoạn 3 lên Bộ Y tế theo đúng yêu cầu của bộ là ngày 4-8.
Song song với quá trình này, nhà sản xuất sẽ hoàn thiện hồ sơ để gửi Bộ Y tế, các hội đồng chuyên gia, đề nghị được cấp phép khẩn cấp cho vắc xin Nano Covax.
Theo thông tin của nhà sản xuất, đã có xấp xỉ 14.000 người tham gia tiêm ngừa vắc xin Nano Covax ở 3 giai đoạn 1, 2, 3. Trong đó giai đoạn 3 gồm: 3a có 1.004 người tham gia, 3b có 12.000 người. Về cơ bản, vắc xin đảm bảo an toàn và sinh miễn dịch tương đương với các vắc xin nhập ngoại đang sử dụng.
Đại diện nhà sản xuất vắc xin cũng cho biết đã có thư ủy quyền cho đại sứ Việt Nam tại Ấn Độ Phạm Sanh Châu tham gia đàm phán để thử nghiệm lâm sàng vắc xin Nano Covax tại Ấn Độ. Ngoài ra còn một số quốc gia đề nghị chuyển giao công nghệ hoặc mua bán thành phẩm Nano Covax. Hiện các đề nghị này vẫn đang ở diện trao đổi.
Ngoài sản phẩm dạng tiêm, Nano Covax còn có sản phẩm sử dụng theo đường xịt mũi.
Thủ tướng Chính phủ cũng đã giao Bộ Y tế và Bộ Tư pháp tháo gỡ các vướng mắc về quy định để có thể cấp phép cho vắc xin.
Luật dược hiện hành yêu cầu thử nghiệm lâm sàng 3 giai đoạn và sản phẩm chứng minh được hiệu quả bảo vệ. Tuy nhiên, nếu chờ đủ các điều kiện này, thời gian chờ đợi sẽ rất lâu.
Kỳ họp Quốc hội vừa qua đã phê chuẩn nghị quyết, giao Thủ tướng quyết định cho phép việc sửa đổi các quy định pháp lý (hiện có vướng mắc là có cho phép cấp phép ở giữa kỳ thử nghiệm lâm sàng giai đoạn 3 và tiếp tục theo dõi chất lượng vắc xin do nhu cầu trong đại dịch hay không).
Các nước cấp phép vắc xin ra sao?
Theo quy trình sử dụng khẩn cấp, nhà sản xuất sẽ thử nghiệm 3 giai đoạn. Tuy nhiên vì là tình huống "khẩn cấp", các nhà sản xuất vừa sản xuất số lượng lớn vắc xin vừa thử nghiệm. Sau khi được cấp phép khẩn cấp, họ sẽ phân phối số vắc xin này.
Việc cấp phép sử dụng khẩn cấp có ý nghĩa tương đối, tức được cấp phép ở Mỹ chưa chắc được cấp phép tương tự ở Việt Nam. Thời gian qua, WHO cũng chỉ xuất bản các tài liệu, hướng dẫn đánh giá lâm sàng cũng như tiêu chuẩn vắc xin cho chính phủ các nước tham khảo, từ đó đưa ra quyết định của riêng quốc gia ấy.
Hiện nay, vắc xin Nano Covax của Việt Nam cũng đang hoàn tất các giai đoạn cuối cùng và đã công khai dữ liệu tiền lâm sàng và lâm sàng. Dữ liệu của Nano Covax được công bố dạng bản thảo (preprint) chưa bình duyệt trên hai kho dữ liệu mở Biorxiv và Medrxiv.
Các bản preprint này là tài liệu nghiên cứu đầy đủ liên quan tới một nghiên cứu. Việc đăng tải công khai preprint sẽ giúp các nhà nghiên cứu "đánh dấu" nghiên cứu của mình để phục vụ vấn đề bản quyền, cũng như đón nhận các trích dẫn, phản hồi... từ các nghiên cứu hoặc bài báo khác.
NHẬT ĐĂNG















Tối đa: 1500 ký tự
Hiện chưa có bình luận nào, hãy là người đầu tiên bình luận