
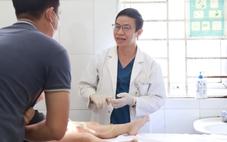
Nghiên cứu sản xuất vắc xin Nanocovax tại Công ty cổ phần công nghệ sinh học dược Nanogen - Ảnh: DUYÊN PHAN
Trước đó, Việt Nam bước vào cuộc chạy đua sản xuất vắc xin phòng chống COVID-19 từ khá sớm với quyết tâm sẽ có được vắc xin "Made in Vietnam" đầu tiên vào cuối tháng 9-2021.
Để đạt được điều này, từ khoảng tháng 5-2020 hai loại vắc xin Nanocovax và Covivac được Bộ KH-CN phê duyệt "danh mục nhiệm vụ khoa học công nghệ cấp quốc gia đột xuất phòng chống dịch COVID-19".
Sau đó có thêm Sputnik V (Nga), VBC-COV19-154 (Mỹ) và Recombinant SARS-CoV-2 Spike Protein (Nhật) được chuyển giao công nghệ sản xuất tại Việt Nam.
"Đứng bánh"!
Vắc xin "Made in Vietnam" đầu tiên được kỳ vọng không ai khác chính là Nanocovax của Nanogen. Tưởng rằng sau phiên họp ngày 18-9-2021 của Hội đồng đạo đức trong nghiên cứu y sinh học quốc gia, Nanocovax được Bộ Y tế phê duyệt cấp phép khẩn cấp nhưng 6 tháng trôi qua, vắc xin này vẫn giậm chân tại chỗ.
Một đại diện của Nanogen khẳng định từ khi COVID-19 bùng phát mạnh trên phạm vi toàn cầu, nhiều nơi vào cuộc sản xuất vắc xin, đó cũng là lúc ý tưởng sản xuất vắc xin của Nanogen được manh nha.
Nhưng phải đến đầu tháng 5-2020, bằng việc đầu tư nguồn lực về tiền bạc, con người, nâng cấp trang thiết bị vật tư, cơ sở hạ tầng để nghiên cứu, bào chế vắc xin... Nanogen mới chính thức được cấp phép nghiên cứu.
"Cho đến nay ở Việt Nam chưa một công ty tư nhân nào nghiên cứu một loại vắc xin có số mẫu thử gần 14.000 người, đặc biệt đây lại là vắc xin phòng COVID-19" - đại diện công ty này nói.
Và trong suốt hai năm qua, với các giai đoạn thử nghiệm, không biết bao lần kiểm tra đánh giá từ Chính phủ, Bộ Y tế, Hội đồng y đức (Ban đánh giá vấn đề đạo đức trong nghiên cứu y sinh học Bộ Y tế)... vắc xin vẫn chưa được ra lò như mong đợi.
Mục tiêu sản xuất 10 triệu liều/tháng, dự kiến đến tháng 1-2022 công suất sẽ được nâng cấp lên, đạt khoảng 30 triệu liều/tháng của Công ty Nanogen vẫn chưa trở thành hiện thực.
Đặc biệt, tháng 6-2021 vì quá sốt ruột, Nanogen có công văn gửi Thủ tướng xin cấp phép khẩn cấp có điều kiện vắc xin Nanocovax, với giá bán chỉ khoảng 120.000 đồng/liều nhưng kiến nghị này được Bộ Y tế đánh giá là "nóng vội".
Trao đổi với Tuổi Trẻ ngày 23-3, nửa tháng sau khi Bộ Y tế có báo cáo Ban Chỉ đạo phòng chống dịch quốc gia cho biết có 3 vắc xin nội đang trong quá trình sản xuất, một thành viên nhóm nghiên cứu thử nghiệm lâm sàng Nanocovax cho biết sau 3 giai đoạn thử nghiệm, có gần 14.000 người đã được tiêm vắc xin Nanocovax các mức liều, trong đó riêng giai đoạn 3b có 12.003 người tham gia.
Tính đến 13-12-2021 khi "cắt dữ liệu", giải mù nghiên cứu, có hơn 100 người trong nhóm đã tiêm mắc COVID-19. Hiệu lực bảo vệ của vắc xin đạt 52%, tức là trên mức tiêu chuẩn theo chuẩn của Tổ chức Y tế thế giới.
Tuy nhiên, vắc xin này vẫn đang dừng ở khâu chờ xác nhận dữ liệu báo cáo cập nhật tiến độ. Và mặc dù Nanocovax đã 2 lần vượt qua "cửa" Hội đồng đạo đức trong nghiên cứu y sinh quốc gia, số phận của vắc xin này ra sao vẫn là một dấu hỏi.
Trong khi đó, Covivac - sản phẩm của Viện Vắc xin và sinh phẩm y tế Nha Trang - cũng bế tắc không kém khi bị tắc ngay sau khi thử lâm sàng giai đoạn 2.
Lý do thời điểm tắc là không tìm đâu ra người chưa tiêm chủng để mời tham gia thử nghiệm lâm sàng giai đoạn 3a và 3b, trong khi bình thường khâu này sẽ diễn ra vào tháng 12-2021 nhưng thời điểm đó hầu hết người dân đã được tiêm chủng ít nhất 1 mũi.
Trong khi đó, vắc xin Arct-154, vắc xin mRNA do một công ty Việt Nam nhận chuyển giao công nghệ, cũng chuẩn bị hoàn tất thử nghiệm lâm sàng giai đoạn 3b.
Dù triển khai nhanh chóng nhưng cơ hội cho vắc xin này tại Việt Nam để tiêm mũi cơ bản (như vai trò của vắc xin trong nghiên cứu thử nghiệm lâm sàng) là hoàn toàn không có.

Nghiên cứu sản xuất vắc xin chống COVID-19 tại Công ty cổ phần công nghệ sinh học dược Nanogen và lộ trình thử nghiệm vắc xin - Ảnh: DUYÊN PHAN
Có tiếp tục nghiên cứu nữa không?
Theo một số chuyên gia, trong lúc "dầu sôi lửa bỏng" phòng chống dịch bệnh, nếu Nanocovax được phê duyệt sẽ góp phần bù đắp được lượng lớn vắc xin đang thiếu hụt của Việt Nam lúc bấy giờ.
"Về tính an toàn, chúng tôi phải giải thích từng ca khi tiêm thử nghiệm và hầu như đều an toàn. Về tính bảo vệ, kết quả lấy máu của tình nguyện viên sau 14 ngày tiêm vắc xin thử trên chủng Vũ Hán, Delta, Alpha... tất cả đều ghi nhận hiệu quả của vắc xin" - đại diện công ty này chia sẻ với Tuổi Trẻ gần đây.
Vậy tại sao vắc xin Nanocovax chưa được cấp phép? Một chuyên gia trong Hội đồng đạo đức khẳng định so với các loại vắc xin trên thế giới thì chất lượng của vắc xin Nanocovax "yếu hơn một chút"; song song đó các yêu cầu của Bộ Y tế hơi chặt chẽ, do đó vắc xin chưa được phê duyệt sử dụng sớm như kỳ vọng của người dân!
"Dù chậm nhưng việc phê duyệt cấp phép cho vắc xin nội chắc chắn bằng cách nào đó phải được tiến hành, bởi nếu không sẽ tạo tiền lệ và khi có một loại dịch bệnh nào đó xảy ra bất ngờ, các doanh nghiệp sản xuất vắc xin trong nước không còn mặn mà để nghiên cứu" - vị này nói.
Cũng theo vị chuyên gia này, dù sắp tới vắc xin nội được phê duyệt cũng đã quá muộn, không còn nhiều ý nghĩa để các doanh nghiệp có được hiệu quả về kinh doanh. "Tuy nhiên, Nhà nước cần ghi nhận đây là nỗ lực của các đơn vị sản xuất, vắc xin này có thể sử dụng để tiêm bổ sung mũi 3, mũi 4 cho một số nhóm người dị ứng với các loại vắc xin nhập khẩu" - vị này nhận xét.
Với vắc xin Covivac, do chưa thử nghiệm giai đoạn 3, chi phí đầu tư không lớn bằng các vắc xin phát triển hay nhận chuyển giao công nghệ khác nhưng cũng là dự án đáng tiếc khi rất được kỳ vọng về hiệu quả và chất lượng.
Nhà sản xuất (Viện Vắc xin và sinh phẩm Nha Trang) cũng đã sẵn có dây chuyền sản xuất vắc xin cúm, có thể chuyển ngay sang sản xuất vắc xin COVID-19. Tuy nhiên việc chậm một khâu sẽ kéo theo nhiều khâu cùng chậm.
Trước những lãng phí về vốn đầu tư, tâm sức của các nhà khoa học, thời gian nghiên cứu thử nghiệm, các chuyên gia đề xuất Bộ Y tế cần sớm hướng các nhà sản xuất vắc xin và đơn vị nhận thử lâm sàng sang thử nghiệm hiệu quả của liều nhắc lại (hiện nay mới thử nghiệm hiệu quả tiêm chủng cho người chưa tiêm vắc xin).
Thử nghiệm thế nào, điều kiện ra sao..., theo các chuyên gia, lại cần đến hướng dẫn của Bộ Y tế.
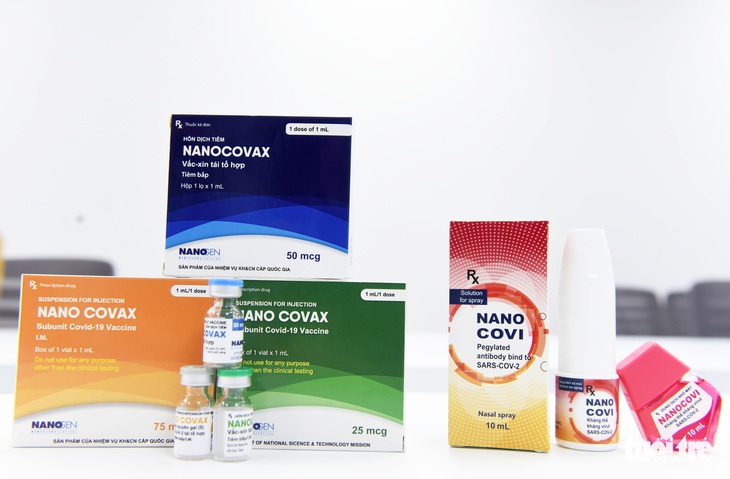
Vắc xin thành phẩm của Nanogen có tên Nanocovax, chia thành ba hàm lượng gồm 25mcg, 50mcg và 75mcg - Ảnh: DUYÊN PHAN
Muốn có một vắc xin phải mất 700 - 800 tỉ đồng trở lên
Theo đánh giá của một chuyên gia lâu năm trong lĩnh vực thử nghiệm lâm sàng vắc xin ở Việt Nam, thế giới đã có "công thức" đầu tư 800 triệu đến 1 tỉ USD để có thể ra đời một vắc xin. Ở Việt Nam, con số này phải từ 700 - 800 tỉ đồng trở lên.
Riêng khâu thử nghiệm lâm sàng chi phí cho một người tham gia thử nghiệm (gồm chi phí theo dõi, xét nghiệm xác định tác dụng vắc xin sau tiêm, vận chuyển mẫu...) cũng khoảng 50 triệu đồng. Ở giai đoạn phát triển vắc xin, tiêm thử nghiệm trên động vật chi phí theo dõi, xét nghiệm cũng lên tới hàng trăm triệu đồng" - chuyên gia này cho biết.
Chuyên gia này nói chưa biết các nhà sản xuất đầu tư như thế nào cho nghiên cứu vắc xin lần này, nhưng ông ước tính đơn vị có số lượng người tham gia thử nghiệm trên 10.000 người, chi phí đầu tư nghiên cứu phát triển vắc xin cũng lên tới 700 - 800 tỉ đồng. Nếu vắc xin cứ "dừng ở trạm" như hiện nay, hàng trăm tỉ đồng này sẽ có nguy cơ "đổ sông đổ bể"
Có tiêm thêm mũi 4, 5 vắc xin COVID-19?
Ông Vũ Đình Thiểm (Viện Vệ sinh dịch tễ trung ương) là người giàu kinh nghiệm trong thử nghiệm lâm sàng vắc xin, cho rằng chính vì hiệu quả của vắc xin COVID-19 không bền nên mới cần tiêm nhắc lại, nhằm bảo vệ người được tiêm khỏi nhiễm bệnh hoặc nếu nhiễm thì bệnh chỉ "thoáng qua".
Ông Thiểm cho rằng bản chất của vắc xin là đưa kháng nguyên (protein của virus, vi khuẩn) vào cơ thể để tạo miễn dịch chủ động, còn người đã mắc bệnh thì cũng sinh kháng thể và có miễn dịch tự nhiên.
Trả lời về việc tiêm nhiều mũi vắc xin COVID-19 và tiêm với lịch như hiện nay thì có ảnh hưởng đến miễn dịch tự nhiên của con người hay không, ông Thiểm cho rằng việc tiêm nhắc lại sẽ giúp củng cố hệ miễn dịch, giúp hiệu quả miễn dịch cao hơn.
Thời gian vừa qua, hiệu quả của vắc xin đã được chứng minh rõ khi tỉ lệ mắc tăng nhiều nhưng tỉ lệ chuyển nặng và tử vong giảm thấp. Nhiều vắc xin như vắc xin ngừa cúm cũng đang tiến hành tiêm nhắc lại hằng năm.
Bộ Y tế ghi nhận gì về vắc xin nội?
Theo báo cáo của Bộ Y tế trình Thủ tướng đầu tháng 3, thời điểm đó Việt Nam đang có 3 ứng viên vắc xin COVID-19 sản xuất trong nước và chuyển giao công nghệ đang triển khai thử nghiệm lâm sàng ở giai đoạn 2 và giai đoạn 3.
Vắc xin Nanocovax của Công ty cổ phần công nghệ sinh học dược Nanogen đã nghiệm thu kết quả thử nghiệm lâm sàng giai đoạn 1 vào tháng 8-2021. Đã được Hội đồng đạo đức trong nghiên cứu y sinh học quốc gia đánh giá kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3, với dữ liệu tính đến ngày 13-12-2021.
Hiện đang tiếp tục thu thập dữ liệu đánh giá tính an toàn, tính sinh miễn dịch và hiệu quả bảo vệ thử nghiệm lâm sàng giai đoạn 2 và giai đoạn 3 của vắc xin theo đề cương nghiên cứu.
Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc và nguyên liệu làm thuốc đã họp thẩm định hồ sơ đăng ký lưu hành vắc xin này và đề nghị công ty sản xuất, các đơn vị nghiên cứu khẳng định về tính chính xác của dữ liệu nghiên cứu.
- Vắc xin Covivac của Viện Vắc xin và sinh phẩm Nha Trang đã đánh giá kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 1; đã hoàn thành tiêm 2 liều của thử nghiệm lâm sàng giai đoạn 2. Đã hoàn thành báo cáo giữa kỳ thử nghiệm lâm sàng giai đoạn 2, đang hoàn thiện đề cương thử nghiệm lâm sàng giai đoạn 3.
- Vắc xin Arct-154 là vắc xin mRNA của Công ty Acturus - Hoa Kỳ được chuyển giao công nghệ về Việt Nam, đã hoàn thành tiêm 2 mũi của thử nghiệm lâm sàng giai đoạn 2 và 3a, 3b, 3c. Đang thu thập, xử lý, phân tích dữ liệu nghiên cứu để đánh giá kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3 phục vụ xem xét cấp giấy đăng ký lưu hành trong trường hợp cấp bách.
DƯƠNG LIỄU
Covivac không chỉ thiếu người thử nghiệm

Thử nghiệm lâm sàng vắc xin Nanocovax được triển khai ở Trung tâm Y tế huyện Bến Lức, tỉnh Long An, do Viện Pasteur TP.HCM thực hiện tháng 2-2021 - Ảnh: DUYÊN PHAN
Chiều 23-3, TS Dương Hữu Thái - viện trưởng Viện Vắc xin và sinh phẩm y tế (IVAC, tại Nha Trang) - cho biết hiện tại IVAC chưa có quyết định làm tiếp hay dừng đối với vắc xin Covivac.
Viện đã báo cáo Bộ Y tế, tùy theo chính sách của Bộ Y tế và Chính phủ để làm tiếp hay dừng. Trước đó, vắc xin Covivac đã được hoàn thành việc tiêm mũi 2 thử nghiệm lâm sàng giai đoạn 2 trên người vào tháng 9-2021 và "đạt yêu cầu về tính an toàn, được dung nạp tốt và sinh kháng thể trung hòa ở mức cao hơn so với vắc xin AstraZeneca".
Trên website của viện, thông qua bài viết "COVIVAC: Sự chìm nổi của một vắc xin Việt" có dẫn ra các nguyên nhân: việc thử nghiệm lâm sàng giai đoạn 3 đối với vắc xin Covivac cần phải được thực hiện với cỡ mẫu lớn hơn, tức quy mô thử nghiệm trên người nhiều hơn và đó là một thách thức.
Bởi "trước hết không còn đủ người chưa tiêm vắc xin hoặc chưa nhiễm COVID-19 để tham gia thử nghiệm... Sự khốc liệt của dịch bệnh và tốc độ tiêm chủng thần tốc ở Việt Nam đã khiến việc thử nghiệm theo phương thức thông thường trở nên không khả thi".
Cũng theo bài viết trên, trường hợp IVAC tiếp tục thử nghiệm hoàn thành, vượt được rào cản thử nghiệm lâm sàng giai đoạn cuối thì "cánh cửa đến quyết định chấp thuận cấp phép khẩn cấp vẫn có thể đóng sập trước mặt.
Bởi quyết định này sẽ đòi hỏi một lượng kinh phí rất lớn, vượt quá khả năng tài chính của một đơn vị hoạt động theo cơ chế sự nghiệp công lập như IVAC".
Cho đến nay, IVAC chỉ mới được Chính phủ đồng ý cấp hơn 8 tỉ đồng từ Quỹ vắc xin để bổ sung cho phần kinh phí còn thiếu ở giai đoạn 1 và 2. Viện đã tìm kiếm nguồn kinh phí để thực hiện giai đoạn 3 nhưng không ra.
P.S.N.











Tối đa: 1500 ký tự
Hiện chưa có bình luận nào, hãy là người đầu tiên bình luận