
Cơ sở sản xuất của Công ty dược Maiden Pharmaceuticals ở ngoại ô New Delhi, Ấn Độ - Ảnh: AFP
Ngày 15-10, Hãng tin Reuters dẫn lời Cơ quan quản lý thực phẩm và dược phẩm quốc gia Indonesia (BPOM) thông báo đang điều tra khả năng diethylene glycol và ethylene glycol trong siro ho tạo ra độc tố trong các nguyên liệu khác được sử dụng làm dung môi trong loại thuốc này.
"Để bảo vệ người dân, BPOM đề ra quy định khi đăng ký thuốc, theo đó mọi sản phẩm siro thuốc dùng cho trẻ em và người trưởng thành không được phép sử dụng diethylene glycol và ethylene glycol", BPOM thông báo ngày 15-10.
Trước đó, Cơ quan y tế Indonesia ngày 12-10 cho biết nước này sẽ điều tra các trường hợp tổn thương thận đang làm chết hơn 20 trẻ em chỉ tính riêng ở thủ đô Jakarta năm nay.
Không chỉ Indonesia, Gambia và Ấn Độ cũng đang điều tra bệnh thận cấp đến nay đã khiến 70 trẻ em ở Gambia thiệt mạng, được cho là liên quan đến loại siro ho của công ty dược Ấn Độ Maiden Pharmaceuticals.
Nhóm điều tra của Tổ chức Y tế thế giới (WHO) phát hiện mức độ diethylene glycol và ethylene glycol "không thể chấp nhận được", có thể gây độc, trong bốn sản phẩm do Maiden sản xuất. Các chất này có thể khiến người dùng gặp các triệu chứng như đau bụng, nôn mửa, tiêu chảy, đau đầu... thậm chí dẫn tới tử vong.
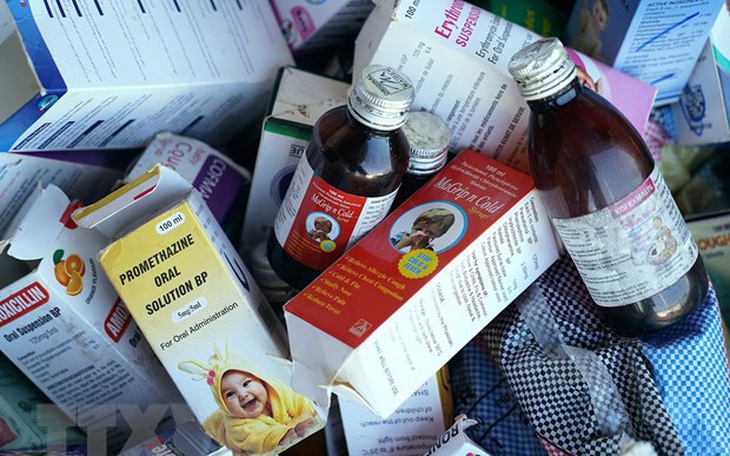
Các sản phẩm này bao gồm Promethazine Oral Solution, Kofexmalin Baby Cough Syrup, Makoff Baby Cough Syrup và Magrip N Cold Syrup. WHO khuyến cáo các nước rà soát và cấm lưu hành những sản phẩm này.
BPOM cho biết bốn loại siro liên quan các trường hợp trẻ tử vong ở Gambia không được đăng ký tại Indonesia.
Về phần Công ty Maiden, hôm 12-10, chính quyền Ấn Độ tuyên bố phát hiện 12 lỗi vi phạm tại một nhà máy của công ty, và đã cho dừng sản xuất thuốc trị ho tại nhà máy của công ty này.












Tối đa: 1500 ký tự
Hiện chưa có bình luận nào, hãy là người đầu tiên bình luận